La malattia di Parkinson è una malattia neurologica degenerativa che comporta una progressiva perdita di funzione principalmente a carico del sistema motorio. Benchè la causa che innesca il processo di degenerazione non sia nota (si ipotizza una interazione fra una predisposizione soggettiva geneticamente correlata e alcuni fattori tossici ambientali) è invece chiaro che le cellule nervose (neuroni) da cui la degenerazione inizia sono quelle di una ristretta area nota come sostanza nigra (così denominata per il colore scuro che visivamente questa zona presenta per l’elevato contenuto in ferro dei suoi neuroni).
Nelle cellule nervose che vanno incontro a degenerazione si trovano spesso dei depositi di una sostanza chiamata sinucleina. La sinucleina è il principale costituente di questi depositi chiamati corpi di Lewy.
Queste cellule utilizzano, come sostanza chimica per interagire con le restanti cellule del sistema nervoso, la dopamina. Ecco quindi che la carenza di dopamina è responsabile dei sintomi di malattia.
La malattia di Parkinson riconosce sintomi non motori e sintomi motori.
I sintomi non motori possono precedere l’inizio della malattia conclamata anche di anni.
I più noti sono:
- la depressione del tono dell’umore;
- la stipsi;
- i disturbi del sonno,
- la riduzione e la perdita dell’ olfatto.
Il coinvolgimento di sistemi e funzioni così diversi non deve stupire. Ciò ricalca la diffusa presenza della dopamina nel nostro sistema nervoso e la complessa attività di regolazione che tale sostanza esercita nei confronti di sistemi diversi tra loro.
Purtroppo si tratta di sintomi poco specifici riconducibili anche a condizioni di malattia non neurologiche: questo, in parte, fa perdere il loro ruolo di marcatori predittivi di malattia. La loro ricerca anamnestica nel paziente che lamenta disturbi motori acquista tuttavia un’ importante funzione diagnostica e contribuisce, laddove i sintomi motori sono ancora molto sfumati, a indirizzare il medico verso la diagnosi.
I sintomi motori sono quelli che caratterizzano la malattia fin dalla prima descrizione fatta dal neurologo James Parkinson alla fine del 1800.
Tremore, rallentamento nei movimenti (bradicinesia), rigidità e instabilità posturale (con maggiore facilità alle cadute) sono i sintomi più noti e in genere sono quelli che più spesso allarmano il paziente conducendolo ad approfondire la sua condizione.
Il tremore è tipicamente un tremore che compare alle estremità degli arti e in condizioni di inattività motoria ovvero ad arto inattivo e appoggiato a una superficie piana e scompare con l’esecuzione di un compito. Il tremore non parkinsoniano, sia esso essenziale o senile o muscolotensivo, si connota per la sua tipica evocabilità nel mantenimento di una postura o nell’esecuzione di un esercizio proprio all’opposto del tremore parkinsoniano.
La bradicinesia è la lentezza a svolgere qualunque compito e viene descritta dal paziente come un aumento del tempo di esecuzione delle attività quotidiane. La bradicinesia, nella sua forma più estrema, può sfociare nella impossibilità a effettuare qualunque attività ovvero nella acinesia. La bradicinesia testimonia della difficoltà del paziente parkinsoniano a pianificare in modo rapido il gesto motorio proprio a causa della carenza di dopamina.
La bradicinesia talora si accompagna alla rigidità muscolare, o ipertono muscolare, altro elemento diagnostico importante che il neurologo può apprezzare durante la visita flettendo ed estendendo le articolazioni oppure osservando nel paziente, invitato a camminare, una riduzione/perdita dei movimenti pendolari delle braccia. La bradicinesia può condurre anche a una modificazione della calligrafia, che si fa più incerta e piccola (micrografia), e a una variazione dell’espressività mimica del volto che appare quasi come una maschera priva di affettività (ipomimia o amimia).

L’ instabilità posturale è la tendenza da parte del paziente a essere meno pronto nel contrastare le perturbazioni del proprio equilibrio. Il sintomo è una diretta conseguenza di quanto visto sopra: la lentezza nel pianificare una strategia motoria per opporsi alla perdita di equilibrio porta il paziente a rispondere in ritardo allo stimolo perturbatore con conseguente caduta.
La diagnosi di malattia di Parkinson è una diagnosi in primo luogo clinica ovvero basata sui sintomi descritti dal paziente e sui segni che il medico rileva alla visita.

La risposta alla terapia e il persistere nel tempo di tale risposta è un ulteriore elemento diagnostico che peraltro permette di differenziare il Parkinson dai parkinsonismi: condizioni degenerative simili al Parkinson per sintomatologia ma dall’andamento più aggressivo e complesso.
Gli esami strumentali hanno solo la funzione di escludere quelle malattie che possono esordire con sintomi parkinsoniani ma che a volte sono sottese a processi non degenerativi come può accadere per malattie tumorali o vascolari. Più specifica è la SPECT cerebrale con l’uso del DATscan.
Brevemente la SPECT è una metodica di medicina nucleare attraverso la quale, la somministrazione di una sostanza metabolicamente attiva marcata con un isotopo radioattivo, permette di seguire la distribuzione del tracciante nell’organismo e di mappare quella determinata attività funzionale.
Nel caso del Parkinson il tracciante (DATscan) misura la densità dei recettori del trasportatore della dopamina nel cervello. Pertanto una perdita di tali recettori si tradurrà in una ridotta attività radioattiva rilevata durante l’esame a comprovare l’ipotesi clinica di malattia sollevata dal neurologo.
L'aumento del rischio di malattia di Parkinson è stato associato all'esposizione a pesticidi, consumo di latticini, anamnesi di melanoma e lesioni cerebrali traumatiche (pugili), mentre è stato riportato un rischio ridotto in associazione con fumo, consumo di caffeina, concentrazioni sieriche di urato più elevate, attività fisica, e l'uso di ibuprofene e altri farmaci comuni.

Il consumo di tè può proteggere dal morbo di Parkinson e questo effetto protettivo è più evidente nelle popolazioni cinesi.
L'incidenza del morbo di Parkinson varia da 5/100.000 a oltre 35/100.000 nuovi casi all'anno. L'incidenza aumenta da 5 a 10 volte dalla sesta alla nona decade di vita. Anche la prevalenza del morbo di Parkinson aumenta con l'età passando da meno dell'1% di uomini e donne di età compresa tra 45 e 54 anni al 4% di uomini e al 2% di donne di età pari o superiore a 85 anni. La mortalità non è aumentata, rispetto agli individui non affetti, nella prima decade dopo la diagnosi di PD, ma aumenta successivamente.
Le donne sono lievemente meno affette rispetto agli uomini probabilmente per meccanismi protettivi legati al diverso assetto ormonale genere correlato.

Le terapie che attualmente si utilizzano per la malattia di Parkinson non agiscono sulla causa (ignota) di malattia ma sui suoi effetti. Esistono farmaci dotati di un potenziale effetto protettivo nei confronti dei fenomeni degenerativi. Tra questi la selegilina, la rasagilina e la safinamide. Il loro ruolo è stato molto controverso nel tempo anche se ad oggi viene comunque confermata, negli studi clinici, una parziale efficacia nel modificare la storia di malattia rallentando l’evoluzione.
I farmaci più significativi in uso sono invece dotati di una attività sintomatica che viene raggiunta con meccanismo sostitutivo sulla carenza di dopamina. In tale contesto si collocano la L-Dopa e i dopaminoagonisti.
La L-Dopa è la sostanza chimica che le cellule nervose impiegano per costruire ovvero per sintetizzare, la dopamina. Si tratta di un aminoacido che viene ricavato dall’alimentazione e che nel paziente parkinsoniano viene somministrato sotto forma di compresse da assumere a stomaco vuoto per ottimizzarne l’assorbimento intestinale. E’ il farmaco che per primo è stato impiegato nella cura della malattia di Parkinson e ad esso si deve il significativo miglioramento della qualità di vita e dell’aspettativa di vita del paziente. Poiché la L-Dopa ha una breve sopravvivenza nel nostro organismo a causa dei numerosi enzimi che la degradano, per contrastare ciò, la ricerca farmacologica nel tempo ha ideato dei prodotti (inibitori dopa decarbossilasi e inibitori COMT) che in una unica compressa coniugano la L-Dopa con gli inibitori di tali enzimi. Ciò ha permesso di allungare la durata dell’effetto farmacologico della L-Dopa regalando al paziente una risposta al trattamento migliore e più stabile.
I dopaminoagonisti (rotigotina, ropinirolo, pramipexolo, apomorfina) sono prodotti di sintesi che mimano l’azione della dopamina. Hanno il vantaggio di non richiedere una trasformazione metabolica da parte delle cellule nervose e, pur avendo una minore potenza rispetto alla L-Dopa nel contrastare i sintomi della malattia, hanno dalla loro una maggiore durata di effetto oltre che la possibilità per alcune molecole (rotigotina) di essere somministrati per via cutanea con l’uso di cerotti da applicare e rinnovare quotidianamente. Si possono utilizzare sia da soli, in monoterapia, sia in associazione alla L-Dopa.
Sia la L-Dopa che i dopaminoagonisti sono gravati da effetti collaterali. Cefalea, sonnolenza e nausea o vomito sono i più frequenti. Altri effetti riguardano la sfera psico comportamentale: si tratta di allucinazioni e alterazione del controllo degli impulsi. Quest’ultimo disturbo, in particolare deve essere oggetto di attenzione, potendo essere causa di comportamenti economicamente pericolosi (come gioco d’azzardo patologico o acquisti compulsivi).
Benché la risposta delle cellule nervose ai farmaci dopaminergici sia conservata nel tempo, l’interazione dei farmaci col processo di malattia, ovvero con il progressivo impoverimento neuronale, genera degli effetti che sono invece variabili. Ciò conduce a riconoscere, nella storia clinica del paziente, due periodi: il periodo della “luna di miele” e il periodo delle fluttuazioni motorie.
Il periodo della luna di miele caratterizza i primi anni di terapia. Dura in genere 5-8 anni durante i quali basse dosi di farmaco consentono un buon controllo dei sintomi e una qualità di vita ottimale. Con la progressione della degenerazione la risposta si fa meno efficace: il paziente inizia a percepire uno scadimento dell’effetto di ogni singola dose (il cosiddetto effetto di fine dose) con il ciclico ripresentarsi, durante la giornata, di momenti in cui la sintomatologia della malattia si ripresenta a indicare la fine dell’effetto.

Progredendo ulteriormente nel tempo, la fine dose viene vissuta come un più repentino passaggio a una condizione di impossibilità a muoversi che diventa all’opposto una iperattività, a volte parassita e scoordinata (discinesie), quando il farmaco viene assunto. Ecco che il paziente oscilla fra due stati opposti: off (o acinesia di fine dose) e on (o iperattività da effetto farmacologico). Purtroppo, non esistono farmaci dedicati al controllo delle fluttuazioni e degli stati ipercinetici e solo l’adeguamento posologico delle terapie, il controllo dell’alimentazione e una rigorosa condotta di vita riescono ancora a dare al paziente una qualità di vita accettabile.
Quando le terapie standard non sono più efficaci si può ricorrere alla somministrazione continua di L-Dopa attraverso micropompe che somministrano il farmaco direttamente nel duodeno (duodopa analogo della L-Dopa) o lo infondono sottocute (apomorfina della classe dei dopaminoagonisti).
Se anche questa linea di intervento fallisce e se il paziente presenta determinate caratteristiche cliniche si potrà proporre la terapia chirurgica che prevede l’impianto, all’interno del cervello, in strutture bersaglio precedentemente identificate, di elettrodi stimolatori collegati con dei generatori elettrici miniaturizzati (simili al pace maker cardiaco) la cui funzione sarà quella di attivare aree cerebrali diversamente non più attivabili farmacologicamente.
Nelle fasi avanzate di malattia occorre prevenire due temibili complicanze:
le cadute rovinose, che possono provocare fratture e conseguente allettamento e ospedalizzazione, e le infezioni specialmente quelle respiratorie. Queste sono spesso la conseguenza della disfagia ovvero della difficoltà del paziente a coordinare adeguatamente la deglutizione con passaggio di alimenti nel tratto respiratorio. Il prolungarsi nel tempo del passaggio di piccole quantità di cibo o saliva determina una condizione di infiammazione respiratoria cronica su cui possono poi sovrapporsi infezioni che, se ripetute, minano le capacità di difesa del paziente esponendolo a peggioramento. La prevenzione si effettua con una modifica del regime dietetico specie per quanto riguarda la consistenza dei cibi che deve essere omogenea e priva di doppie consistenze (solido/liquido), impiegando addensanti e nei casi estremi ricorrendo al sondino naso gastrico o alla PEG.
Non esistono stili di vita particolari per prevenire lo sviluppo della malattia di Parkinson.
Il fumo e l’uso di caffè sono correlati con una minore incidenza di malattia anche se la associazione tra fumo e tumore del polmone e malattia vascolare rende controproducente questo strumento in termini di prevenzione. Una volta ricevuta la diagnosi è dimostrato che l’attività fisica e l’uso di sostanze a funzione antiossidante hanno un impatto nel rallentare il progredire della degenerazione dei neuroni.
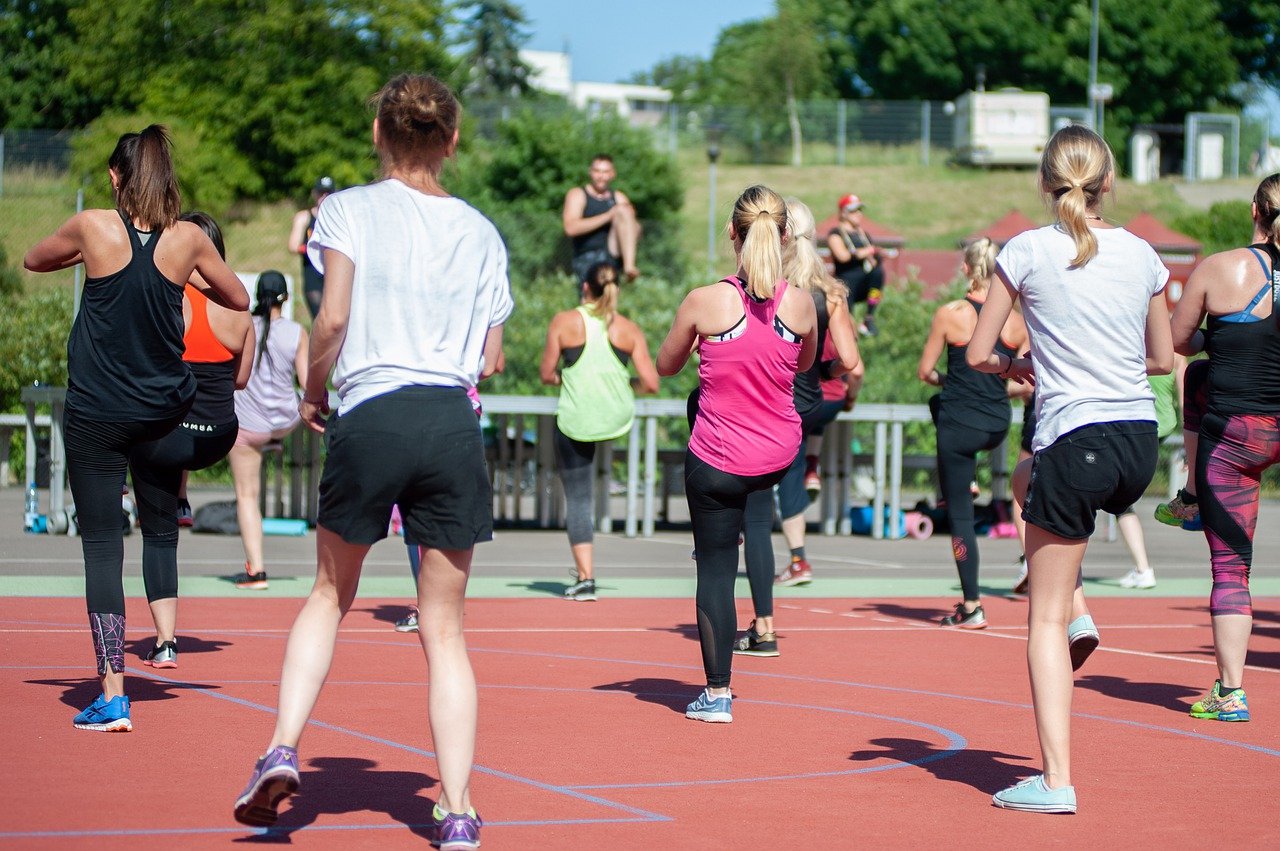
Nell’ambito dell’attività fisica il cammino svolto quotidianamente per almeno mezzora al giorno e con l’uso dei bastoncini (nordic walking) correla positivamente con un miglioramento della qualità di vita del paziente. Altra attività utile è la danza (specie tango e danza irlandese) la cui funzione è duplice: socializzante e terapeutica anche paradossalmente nei pazienti che appaiono più compromessi. La musica e il ritmo spesso riescono a scardinare le difficoltà del paziente a generare autonomamente il movimento tanto che, quasi magicamente, vi sono pazienti bloccati che riescono a ballare con disinvoltura. Anche discipline come il Tai Chi o la idrochinesiterapia migliorano la presa di contatto del paziente col proprio corpo ottimizzando il controllo sul corpo stesso e riducendo il timore delle cadute (specie per quel che concerne la ginnastica in acqua).

Cervello
Malattia di Parkinson il ruolo delle associazioni
Nelle malattie croniche il percorso attraverso cui il paziente deve imparare a convivere con la malattia è lungo.
I farmaci spesso alleviano le difficoltà ma da soli non rendono meno gravosi i problemi assistenziali che malato e caregiver devono affrontare.
La creazione di associazioni in cui paziente, caregiver, medico, psicologo, fisioterapista e infermiere cooperano apertamente per apprendere reciprocamente quelle che possono essere le necessità più importanti per rendere più agevole la quotidianità è un elemento costitutivo della cura.
In questa chiave interpretativa il termine cura sviluppa tutta la sua valenza etica più profonda e trasforma la malattia in esperienza vitale alleviando il peso legato al modificarsi della fisicità imposto dalla malattia.
Dottor Franco Bruno Grassi
La malattia è una condizione dell’esistenza che non deve condizionare l’esistenza


